Kooldioxide: klimaat, eigenschappen, afvang en opslag
Deze pagina beschrijft
• De fysische eigenschappen van CO$_2$, welke belangrijk zijn voor transport en opslag.
• Een introductie op klimaat en CO$_2$.
• CO$_2$ afvang en opslag: de technologie, de ontwerpkeuzes en de maatschappelijke discussie.
Eigenschappen van CO$_2$
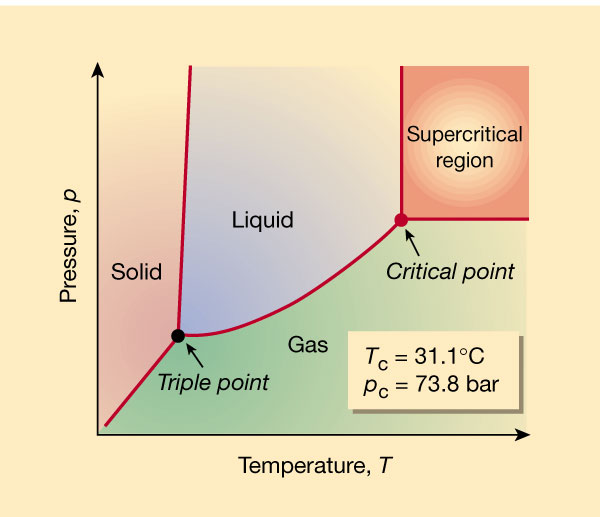
Kooldioxide, CO$_2$, is een belangrijk broeikasgas. De broeikaseffect-versterkende werking van CO$_2$ is veel geringer dan die van bijvoorbeeld methaan of lachgas, maar het gaat om reusachtige hoeveelheden, omdat CO$_2$ vooral vrijkomt bij verbranding van fossiele brandstoffen, en dat is nog steeds de belangrijkste vorm van energievoorziening in de wereld. Natuurlijk komt er ook CO$_2$ vrij bij verbranding van biomassa, maar dat is kort-cyclisch CO$_2$ dat weer opgenomen kan worden door groeiende planten, aannemend dat het landoppervlak voor plantengroei (natuur en landbouw) gelijk blijft. De mens veroorzaakt per jaar zo’n 8 miljard ton CO$_2$ emissies naar de atmosfeer. Daarvan wordt 55% opgeslagen in oceanen en planten; de rest blijft in de atmosfeer. Op zo’n 100 meetstations over de hele wereld wordt de concentratie van CO$_2$ in de atmosfeer gemeten. Sinds het begin van de metingen in 1958 is de concentratie gestegen van 315 ppm naar 417 ppm in 2022.Bij kamertemperatuur en atmosferische druk is CO$_2$ gasvormig. Als je bij atmosferische druk de temperatuur verlaagt, gaat CO$_2$ bij -78,5 $^o$C over van de gasfase naar de vaste fase (koolzuurijs). Bij atmosferische druk kan vloeibaar CO$_2$ niet bestaan. Het tripelpunt, dat is de combinatie van temperatuur en druk waarbij CO$_2$ zowel gasvormig, vloeibaar als vast kan zijn ligt bij -56,4 $^o$C en 5,11 atmosfeer. In onderstaand fasendiagram van CO$_2$ zie je, behalve het tripelpunt, nog een opvallend punt: het zogenaamde kritische punt, waarbij gasvormig en vloeibaar CO$_2$ overgaan naar een andere ‘toestand’: de superkritische fase.
Superkritische CO$_2$ heeft zowel chemisch als fysisch andere eigenschappen dan vloeibaar of gasvormig CO$_2$. Je zou gemakshalve kunnen zeggen dat het qua fysische eigenschappen het meeste lijkt op gasvormig CO$_2$ (het stroomt gemakkelijk door een zeer lage viscositeit) en qua chemische eigenschappen en dichtheid meer lijkt op vloeibaar CO$_2$ (het heeft een veel hogere dichtheid dan de gasfase, hoewel minder hoog dan die van de vloeibare fase). De bijzondere eigenschappen van superkritisch CO$_2$ worden onder meer nuttig gebruikt in de voedings- en geneesmiddelenindustrie. Zo wordt superkritisch CO$_2$ tegenwoordig bijvoorbeeld gebruikt om cafeïne te extraheren uit koffie (vroeger werd decaf gemaakt door extractie van cafeïne met organische oplosmiddelen).
Klimaat en CO$_2$ concentratie
De ontwikkeling van de CO$_2$ concentratie in de atmosfeer geeft aanleiding tot zorgen over anthropogene klimaatverandering (klimaatverandering die veroorzaakt wordt door de mens, anders dan door natuurlijke processen), en over de ecologische en economische schade die daarvan het gevolg kan zijn (bijvoorbeeld door zeespiegelrijzing en extreme stormen). Daarom is er klimaatbeleid ontwikkeld. Dat heeft ten doel de wereldgemiddelde temperatuurstijging tot niet meer dan 2 graden te beperken (ten opzichte van het pre-industriële tijdperk).Dat de concentratie van CO$_2$ in de atmosfeer niet constant is, komt niet als een verrassing. Bomen en planten nemen in de zomer CO$_2$ op uit de atmosfeer, via het proces van fotosynthese. In de herfst en winter, als de bladeren vallen en planten afsterven, stopt dit proces. Er is dus een seizoenscyclus in de atmosferische CO$_2$ concentratie, met een verschil tussen zomer en winter in de orde van 10 ppm (afhankelijk van de meetlocatie). Onderzoek van luchtbelletjes in ijskernen laat zien dat de atmosferische CO$_2$ concentratie ook fluctueert op een veel langere tijdschaal, met een tijdconstante van 150.000 à 200.000 jaar. Die fluctuatie beweegt zich, over de periode waarover we kunnen terugkijken (tot zo’n 450.000 jaar geleden), in een bandbreedte tussen de 200 ppm en 300 ppm. De huidige CO$_2$ concentratie van circa 400 ppm is een nieuw fenomeen, waarvan we mogen aannemen dat het door menselijk handelen is veroorzaakt: het grootschalig ontginnen van bossen en moerassen voor agrarisch landgebruik en het grootschalig verbranden van fossiele brandstoffen voor industriële en andere doeleinden.
De natuurlijke langzame fluctuatie van de atmosferische CO$_2$ concentratie lijkt samen te vallen met de afwisseling van ijstijden (glacialen) en relatief warme perioden (interglacialen). Dat heeft waarschijnlijk te maken met onregelmatigheden in de elliptische baan van de aarde rond de zon, en met variaties in de stand van de aardas in de ruimte en ten opzichte van het elliptische baanvlak rond de zon. Overigens waren ook de ijstijden zelf geen uniforme perioden van koude: ook binnen de ijstijden wisselden perioden van koude (stadialen) en warmere perioden (interstadialen) elkaar af. Het mechanisme dat voor die instabiliteit verantwoordelijk wordt gehouden is te vinden in het patroon van oceaanstromingen. In de huidige tijd transporteert de warme golfstroom relatief warm en zout water vanuit de tropen naar het noorden. Daar koelt het af, waarna het relatief zware (want extra zoute) water naar de bodem zinkt en over de oceaanbodem terugstroomt naar het zuiden. Dit mechanisme van thermo-haliene circulatie staat bekend als de oceanische warmtepomp. Die circulatie is echter niet stabiel. Als er in warme perioden veel poolijs smelt, kan de laag koud en zoet water aan het oceaanoppervlak zich zo ver uitbreiden dat die het warme zoute water uit de tropen tegenhoudt. Als dat verschijnsel optreedt stopt de warmtepomp en begint er een nieuwe koudeperiode. De noordelijke zeeën worden dan geleidelijk weer kouder en de gletsjers zullen weer aangroeien.
Er wordt wel gespeculeerd dat het afsmelten van de Groenlandse ijskap een nieuwe ijstijd zou kunnen inluiden, voorafgaande aan een nieuw tijdperk van definitieve opwarming van de aarde. Sinds 2011 zien we bijna elke zomer dat er uitgebreide smelt optreedt over het hele oppervlak van de ijskap van Groenland. Op 10 december 2019 verscheen er een alarmerende publicatie in Nature over het ijsverlies in Groenland. Het ijsverlies sinds 1992 is 3800 miljard ton, goed voor een wereldwijde stijging van de zeespiegel met 10,6 mm. Dat ijsverlies voltrekt zich steeds sneller: van gemiddeld 33 miljard ton per jaar in de jaren 90 van de vorige eeuw tot 254 miljard ton per jaar in het afgelopen decennium (met een piek van 335 miljard ton per jaar in 2011). Die versnelling van het ijsverlies past in het worst case scenario van het Inter-Governmental Panel on Climate Change (IPCC), dat een wereldwijde zeespiegelstijging van 67 cm voorspelt in het jaar 2100.
Er zijn dus gegronde redenen om ons zorgen te maken over de toenemende concentratie van CO$_2$ en andere broeikasgassen in de atmosfeer. CO$_2$ is op zichzelf niet giftig voor het leven op aarde, althans niet in een concentratie in de 300-400 ppm range. Pas wanneer de concentratie toeneemt tot enkele volumeprocenten in de lucht die wij inademen, treden er fysiologische effecten op; concentraties van 8 à 10 volume procent zijn dodelijk. Voor beroepsmatige blootstelling is de grenswaarde gesteld op 0,5 vol%. We kennen CO$_2$ in het dagelijks leven als de ‘luchtbelletjes’ in frisdranken, of als blusmateriaal in sommige brandblussers. In de natuur is CO$_2$ het product van organische afbraakprocessen (bijv. in veenbodems) en van vulkanische activiteit. In sommige kratermeren kunnen door vulkanische processen gasbellen van CO$_2$ ontstaan, die tot instabiliteit leiden: als de gasbel uiteindelijk ontsnapt, stroomt het gas (dat zwaarder is dan lucht) langs de berghelling naar beneden. Dit fenomeen wordt verantwoordelijk gehouden voor de dood van 1700 mensen bij het Nyosmeer in Kameroen in 1986.
Met het Nederlandse Klimaatakkoord wordt beoogd de totale uitstoot aan broeikasgassen in 2030 teruggebracht te hebben naar 51% van de uitstoot in 1990, een vermindering van 228 Mton naar 116 Mton. In het Klimaatakkoord zijn afspraken gemaakt over de taakstelling van elke sector in het verminderen van de uitstoot van CO$_2$ en andere broeikasgassen. Zoals je ziet is ‘onze’ sector: Energie en Industrie, verantwoordelijk voor het leeuwendeel (ongeveer de helft) van de uitstoot. De sectoren “Elektriciteit” en “Industrie” hebben een emissiereductiedoelstelling van resp. 20,2 Mton en 14,3 Mton CO$_2$-equivalenten in 2030. Als ze die halen resteert er in 2030 nog steeds een behoorlijke jaarlijkse emissie van resp. 12,4 Mton en 35,7 Mton CO$_2$ equivalenten. Voor 2050 wordt een vermindering van de uitstoot beoogd met 90% ten opzichte van 1990. Hoe die reductie tot stand moet komen, is nog niet ingevuld.
Afvang en opslag van kooldioxide (CCS)
Het bevorderen van energiebesparing (bijv. door energieneutrale woningen te bouwen) en het gebruik van duurzame energie (uit zon, wind, water en biomassa) zijn belangrijke componenten van het klimaatbeleid. Het tempo waarmee langs die wegen structurele reductie van CO$_2$ emissies bereikt kan worden, is echter niet voldoende om de klimaatdoelstellingen te halen. Daarom wordt er ook veel onderzoek gedaan naar technieken om CO$_2$ op te vangen en het veilig op te slaan, zodat het in geen geval in de atmosfeer terecht komt. We spreken hier van CCS: Carbon Capture and Storage. Carbon Capture and Storage (CCS) is een verzamelnaam voor verschillende (combinaties van) technieken om te voorkomen dat de CO$_2$ die ontstaat bij de verbranding van fossiele brandstoffen, in de atmosfeer terecht komt. Er wordt wel gesproken van ‘schoon fossiel’ als energievoorziening uit fossiele brandstoffen gecombineerd wordt met CCS.In de industrie en de energiesector is de uitstoot vooral afkomstig van grootschalige stationaire bronnen. Dat is een heel ander beeld dan in bijv. het verkeer en vervoer, waar de uitstoot vooral gedistribueerd plaatsvindt, uit een groot aantal, relatief kleine, mobiele bronnen. Bij de grootschalige stationaire bronnen in ons domein is, anders dan bij mobiele bronnen, het afvangen van CO$_2$ aan de bron een optie die technisch haalbaar is.
Afvang
Om bij een elektriciteitscentrale die kolen, gas of olie verstookt CO$_2$ emissies te voorkomen bestaan de volgende mogelijkheden:• CO$_2$-verwijdering na verbranding (post-combustion). Dat kan a) uit de rookgassen na verbranding met lucht of b) na verbranding met zuivere zuurstof (oxyfuel)
• CO-verwijdering vóór verbranding (pre-combustion). Dat kan alleen wanneer eerst syngas (een mix van CO en H$_2$) wordt gemaakt, bijvoorbeeld door kolen eerst te vergassen.
Voor bestaande centrales komt alleen de eerste route in aanmerking. In het eerste geval (post combustion) moet je CO$_2$ verwijderen uit de rookgassen die vrijkomen bij de verbranding. Dat betekent dat je een enorm volume rookgassen moet zuiveren van CO$_2$. In de praktijk betekent dit dat alle rookgas door een gaswasser wordt geleid, die selectief CO$_2$ afvangt. Een alternatieve post-combustion route is om de verbranding in de centrale niet uit te voeren met lucht, maar met zuivere zuurstof (oxyfuel). Dan komt er bij de verbranding alleen CO$_2$ en water vrij en is er geen gaswasser nodig. De kosten die je bespaart op de gaswasinstallatie, gaan dan (grotendeels) zitten in de luchtscheidingsinstallatie die nodig is voor de bereiding van zuivere zuurstof. In alle gevallen kost de verwijdering van CO$_2$ na verbranding veel energie.
De pre-combustion route verdient speciale vermelding: hier wordt feitelijk synthesegas (syngas) gemaakt. Dat is een mengsel van koolmonoxide (CO) en waterstof (H$_2$). Syngas wordt in raffinaderijen gemaakt voor de productie van waterstof (die nodig is om uit zware olie toch zoveel mogelijk ‘lichte‘ producten als bijvoorbeeld benzine te maken). In de chemische industrie wordt syngas gemaakt uit aardgas voor de productie van methanol. Met betrekking tot elektriciteitscentrales, zou dat ook kunnen met aardgascentrales en door vergassing van kolen. De kolen worden vergast (gasification) en met behulp van stoom omgevormd (steam reforming) naar synthesegas. Uit het synthesegas wordt CO$_2$ verwijderd, waarna alleen het waterstofdeel resteert voor de verbranding/elektriciteitsproductie.
Kosten en efficiëntie van afvangen
Als je bedenkt dat elektriciteitscentrales een economische levensduur hebben van zo’n 40 jaar, dan snap je ook dat de meeste centrales niet anders kunnen dan een installatie voor post-combustion verwijdering van CO$_2$ bouwen. Ze kunnen niet zomaar overschakelen naar de oxyfuel of de pre-combustion route: in beide gevallen vragen de verbrandingscondities (bijv. hogere verbrandingstemperatuur) om een ander ontwerp van de verbrandingskamer (en een andere inrichting van de process control systemen). De verwijdering van CO$_2$ uit de rookgassen is echter ook een kostbare zaak: het absorptiemiddel (meestal een amine) waarin CO$_2$ wordt afgevangen, moet geregenereerd worden (door verhitting). Per ton CO$_2$ kost dat ongeveer 3 à 4 GJ. Het CO$_2$ dat daarbij vrijkomt wordt afgevangen en gecomprimeerd voor transport. Het schone absorptiemiddel wordt teruggevoerd voor hergebruik in de gaswasser. Voor een gemiddelde kolengestookte elektriciteitscentrale van 1,1 GWe praat je al gauw over een rookgasstroom van 3 miljoen m3 per uur, die ‘gewassen’ moet worden in een absorptietoren met een diameter van 32 meter. De totale extra investering bedraagt honderden miljoenen euro's (300-600). De energie die nodig is voor de rookgasreiniging vertaalt zich in een 12-14% efficiency verlies van de centrale als geheel. Met de huidige prijzen voor CO$_2$-emissierechten kunnen al die extra kosten (in de orde van 30 tot 35 Euro per ton vermeden CO$_2$ emissie) bij lange na niet worden terugverdiend. Het mag dan ook geen verbazing wekken dat er nog weinig gebeurt op het gebied van CO$_2$ verwijdering bij elektriciteitscentrales. Wereldwijd zien we wel dat er grote stappen worden gemaakt in CO$_2$-emissiereductie door het overschakelen van steen- en bruinkool naar aardgas.Het kostenplaatje kan verbeteren met nuttige toepassingen voor afgevangen CO$_2$, waarmee een deel van de verwijderingskosten kan worden gedekt. Tot de mogelijke nuttige toepassingen valt bijv. de toepassing als nutriëntgas in de glastuinbouw. Dat gebeurt in Nederland in het Westland, waar via een oude pijpleiding van defensie (tussen Rotterdam en Beverwijk) CO$_2$ aangevoerd naar enkele glastuinbouwlocaties. Het CO$_2$ in deze leiding is (grotendeels) afkomstig uit Pernis, uit een waterstofproductie-installatie die waterstof maakt voor de kraker van Shell (hydrogenerend kraken van aardolie). Feitelijk is dit een installatie die waterstof maakt uit aardgas (door steam reforming van synthesegas, zoals eerder beschreven voor de pre-combustion route voor CO$_2$ verwijdering), en waarbij vrijwel zuiver CO$_2$ vrijkomt. Het CO$_2$ wordt als gas gedistribueerd op een druk van 30 bar. Het is daarbij overigens niet zo dat alle extra aangevoerde CO$_2$ daadwerkelijk door de planten in de kas wordt opgenomen; een groot deel verdwijnt alsnog naar de atmosfeer bij het ventileren van de kas.
Een andere nuttige toepassing van CO$_2$ is die in de olie- en gaswinning zelf. Door CO$_2$ in een reservoir te pompen kan er meer aardolie (of aardgas) worden geproduceerd (Enhanced Oil Recovery – EOR). Op vergelijkbare manier kan er zo uit oude steenkoolmijnen methaan (aardgas) worden geproduceerd. Je kunt je natuurlijk afvragen of deze toepassingen houdbaar zijn, als we tegelijkertijd bezig zijn onze afhankelijkheid van fossiele brandstoffen terug te dringen. Vooral in de VS wordt CO$_2$ ingezet voor EOR.
Transport
Afgevangen kooldioxide wordt vervoerd via pijpleidingen of schepen naar de opslag. Als CO$_2$ bij elektriciteitscentrales of andere installaties wordt afgevangen en getransporteerd moet worden naar een opslaglocatie, dan moet er, afhankelijk van de hoeveelheden en de afstand die overbrugd moet worden, een keuze worden gemaakt om het ofwel als gecomprimeerd gas te transporteren, ofwel (bij aanzienlijk hogere temperatuur en druk) als superkritisch CO$_2$. Voor grote hoeveelheden en lange afstanden is de superkritische fase te prefereren vanwege de lagere stromingsweerstand en de veel hogere dichtheid dan die van gecomprimeerd gas. Zo wordt er in de VS superkritisch CO$_2$ over grote afstanden getransporteerd van raffinaderijen naar olie- en gasproductievelden, waar het CO$_2$ vervolgens wordt geïnjecteerd voor enhanced oil/gas recovery. In Nederland loopt er een CO$_2$ transportleiding van Shell Pernis (waar het vrijkomt als bijproduct van de waterstoffabriek) naar tuinders in Bergschenhoek, Berkel & Rodenrijs en Bleiswijk, die het gebruiken als nutriënt voor de planten in hun kassen. In dit geval wordt CO$_2$ getransporteerd als gas, bij 40 bar.Hoe dan ook, na verwijdering/afvangen van CO$_2$ moet het getransporteerd worden naar de locatie waar het nuttig gebruikt kan worden of waar het duurzaam wordt opgeslagen. In de pijpleiding door het Westland wordt CO$_2$ als gecomprimeerd gas (30 bar) getransporteerd. Over lange afstanden (honderden kilometers) is het niet gebruikelijk voor transport als gas te kiezen. Dan wordt er meestal gekozen voor transport in superkritische toestand. In het fasendiagram van CO$_2$ (zie eerder op deze pagina) kun je zien dat CO$_2$ bij atmosferische druk alleen maar kan voorkomen in vaste (koolzuurijs) of gasvormige toestand, afhankelijk van de temperatuur. Bij kamertemperatuur onder atmosferische druk is het altijd gasvormig. Bij het zogenaamde tripelpunt kunnen de gasvormige, vloeibare en vaste fasen van CO$_2$ naast elkaar bestaan. Bij hogere temperaturen en drukken bereiken we in het fasendiagram het kritische punt, waarbij een nieuwe fase kan bestaan: de superkritische fase. In de superkritische fase gedraagt CO$_2$ zich heel anders dan in de eerder genoemde fasen. Qua dichtheid is superkritisch CO$_2$ (800 à 900 kg/m3) vergelijkbaar met vloeibaar CO$_2$ (1200 kg/m3), maar het is feitelijk onjuist om van een vloeistof te spreken. Superkritisch CO$_2$ kan vrijwel wrijvingsloos, dus zeer energie-efficiënt, getransporteerd worden (als ware het een gas) en daarom, in combinatie met de relatief hoge dichtheid, wordt voor lange-afstandstransport voor deze vorm gekozen (ondanks de relatief hoge druk).
Opslag
Kooldioxide kan worden opgeslagen in lege aardgasvelden, in lege zoutcavernes en in diepe aquifers. In de loop der tijd lost het op in het daar aanwezige (brakke) formatiewater, waarna het geadsorbeerd wordt aan het formatiegesteente en tenslotte door mineralisatie (waarbij carbonaatgesteenten ontstaan) voorgoed geïmmobiliseerd wordt. Dat proces kost duizenden jaren.Als we afgevangen CO$_2$ duurzaam willen onttrekken aan de atmosfeer, dan rest eigenlijk alleen de optie van geologische opslag in lege olie- of gasvelden, in offshore aquifers of in mineralen. In het aardgascollege hebben we al even besproken dat het Noorse Statoil als eerste bedrijf op commerciële schaal CO$_2$ opslaat, dat is verwijderd uit het aardgas dat Statoil wint uit het Sleipnerveld op de Noordzee. Het verwijderde CO$_2$ wordt ter plaatse opgeslagen in een zoutwater aquifer in de Utsiraformatie. Bij geologische opslag in een poreuze gesteentelaag (zoals een leeg olie- of gasveld) wordt CO$_2$ onder druk geïnjecteerd; in eerste instantie ontstaat er een vloeistofbel in die gesteentelaag, die wordt tegengehouden door een ondoordringbare laag boven het poreuze formatiegesteente. Geleidelijk aan wordt het vloeibare CO$_2$ geabsorbeerd in de poriën van de poreuze formatie, als in een spons. In deze fase van het opslagproces wordt gesproken van structural trapping. Daarna treden geleidelijk andere mechanismen in werking: de fysische absorptie in het gesteente schrijdt voort tot in de kleinste poriën (residual trapping), waarna chemische opslagmechanismen hun werk kunnen gaan doen: dissolution trapping en mineral trapping. Die mechanismen treden pas in werking op zeer lange tijdschaal (denk aan honderd jaar voor dissolution trapping en aan duizenden jaren voor mineral trapping). Op de Noordzee zijn er heel veel lege olie- en gasvelden die zo als ‘laatste rustplaats’ voor afgevangen CO$_2$ zouden kunnen dienen.
Olivijn
Deltares werkt aan een alternatieve oplossing, waarbij het mineraal olivijn wordt ingezet om CO$_2$ uit de atmosfeer te vangen (naar een idee van Olaf Schuiling, emeritus hoogleraar van de Universiteit Utrecht). Olivijn is een van de meest voorkomende mineralen in de aardkorst. Onder invloed van water en CO$_2$ verweert het langzaam tot kalk (calciumcarbonaat). Bij de proeven die nu worden uitgevoerd wordt olivijn uit verschillende mijnen getest, wordt de korrelgrootte van het materiaal gevarieerd, en wordt de zuurgraad van het water gevarieerd. Er is voorlopig nog geen sprake van grootschalige toepassing, maar het is denkbaar dat onze landbouwgronden en wegbermen in de toekomst bemest gaan worden met olivijnkorrels die dan, behalve voor de kalkbemesting, ook zullen zorgen voor afvang van CO$_2$ uit de atmosfeer.Maatschappelijke discussie
Er is een heel scala aan argumenten voor en tegen CCS in het kader van klimaat, energie, milieu, economie, veiligheid en ethiek. TNO heeft deze argumenten in kaart gebracht in de Argumentenkaart CO2-afvang en -opslagw. Er is een grote diversiteit aan argumenten voor en tegen. CCS kan helpen bij het behalen van klimaatdoelstellingen, het belang voor CCS is te zien in de grote reductiebijdrage van 18 Mton in de indicatieve toedeling voor reductie tot 2030 Regeerakkoord (2017)w. Maar er zijn ook argumenten tegen, bijvoorbeeld omtrent de kosten die aanzienlijk zijn. De benodigde investering kan dan niet naar andere maatregelen. Een eerder CCS project in Barendrecht is berucht geworden vanwege de publieke weerstand: zonder maatschappelijk draagvlak bleek de uitvoer niet mogelijk Barendrecht CCSw. Onafhankelijk onderzoek heeft aangetoond dat de opslag veilig plaats zou kunnen vinden, het is echter een nieuwe techniek die nog nooit grootschalig is toegepast, waardoor de risico's niet volledig bekend zijn.Meer weten:
• Nuttige toepassingen van CO2w
Bronnen
Leitner 2000w, Walter Leitner, Green chemistry: Designed to dissolve, in: Nature 405, 129-130 (11 May 2000), doi:10.1038/35012181Laatste wijziging: 11-01-2024

Deze publicatie valt onder een Creative Commons licentie. Zie hiervoor het colofon.

Deze publicatie valt onder een Creative Commons licentie. Zie hiervoor het colofon.