Secundaire luchtverontreiniging
Fotochemische reacties spelen een hoofdrol bij het ontstaan van secundaire luchtverontreining. Secundaire luchtverontreiniging is een verzamelterm voor verschillende vormen van luchtverontreiniging die ontstaan door een fotochemische reactie tussen de stoffen behorend tot primaire luchtverontreiniging of door een reactie met andere stoffen die al aanwezig zijn in de atmosfeer. Zo worden SO2 en NOx bijvoorbeeld omgezet in zwavelzuur (H2SO4) resp. salpeterzuur (HNO3) en verlaten de atmosfeer vervolgens in de vorm van zure regen.
Bij deze fotochemische reacties speelt het hydroxylradicaal (•OH) een belangrijke rol. Hydroxylradicalen worden in een schone atmosfeer onder invloed van licht gevormd uit ozon en water:
O3 — hν→ O2 + O•
O• + H2O → 2 •OH
Er worden maar zeer weinig hydroxylradicalen gevormd in de atmosfeer, maar doordat ze erg reactief zijn spelen ze een hoofdrol bij de verwijdering van SO2, NOx en CO uit de atmosfeer. De verwijdering van NOx (NO en NO2) verloopt als volgt:
NO + O• → NO2
NO2 + •OH → HNO3
De verwijdering van SO2 verloopt vergelijkbaar:
SO2 + •OH → HSO3•
HSO3• + O2 + H2O → H2SO4 + HO2•
In de laatste reactie wordt een hydroperoxylradicaal (HO2•) gevormd, dat bijvoorbeeld met zuurstof tot ozon en een nieuw hydroxylradicaal reageert:
HO2• + O2 → •OH + O3
Ten slotte reageert koolmonoxide ook met een hydroxylradicaal tot kooldioxide en een waterstofradicaal, dat direct met water reageert:
CO + •OH → CO2 + H•
H• + H2O → •OH + H2
De verwijdering van SO2 en CO met hydroxylradicalen loopt dus door totdat er geen SO2 en/of CO meer aanwezig is. Immers, het hydroxylradicaal wordt steeds, via het hydroperoxylradicaal, teruggevormd en fungeert als het ware als chemisch katalysator van de omzetting van SO2 en/of CO.
De voorgaande cyclus van reacties kan verder worden geïntensiveerd door de aanwezigheid van sporen van bepaalde metalen, zoals ijzer (Fe) en mangaan (Mn). De tweewaardige ionen van deze metalen, Fe2+ en Mn2+ zijn erg reactief. De volgende serie reacties treedt op met ijzer:
2Fe2+ + 2H+ + O2 → 2Fe3+ + H2O2
Fe2+ + H+ + H2O2 → Fe3+ + •OH + H2O
Behalve de eerder beschreven reactie van het hydroperoxylradicaal met zuurstof kan het hydroperoxylradicaal ook uiteenvallen in zuurstof en waterstofperoxide:
2 HO2• — hν→ O2 + H2O2
Uiteindelijk wordt de cirkel rond gemaakt door reductie van het ijzer onder invloed van licht:
Fe3+ + OH- — hν→ Fe2+ + •OH
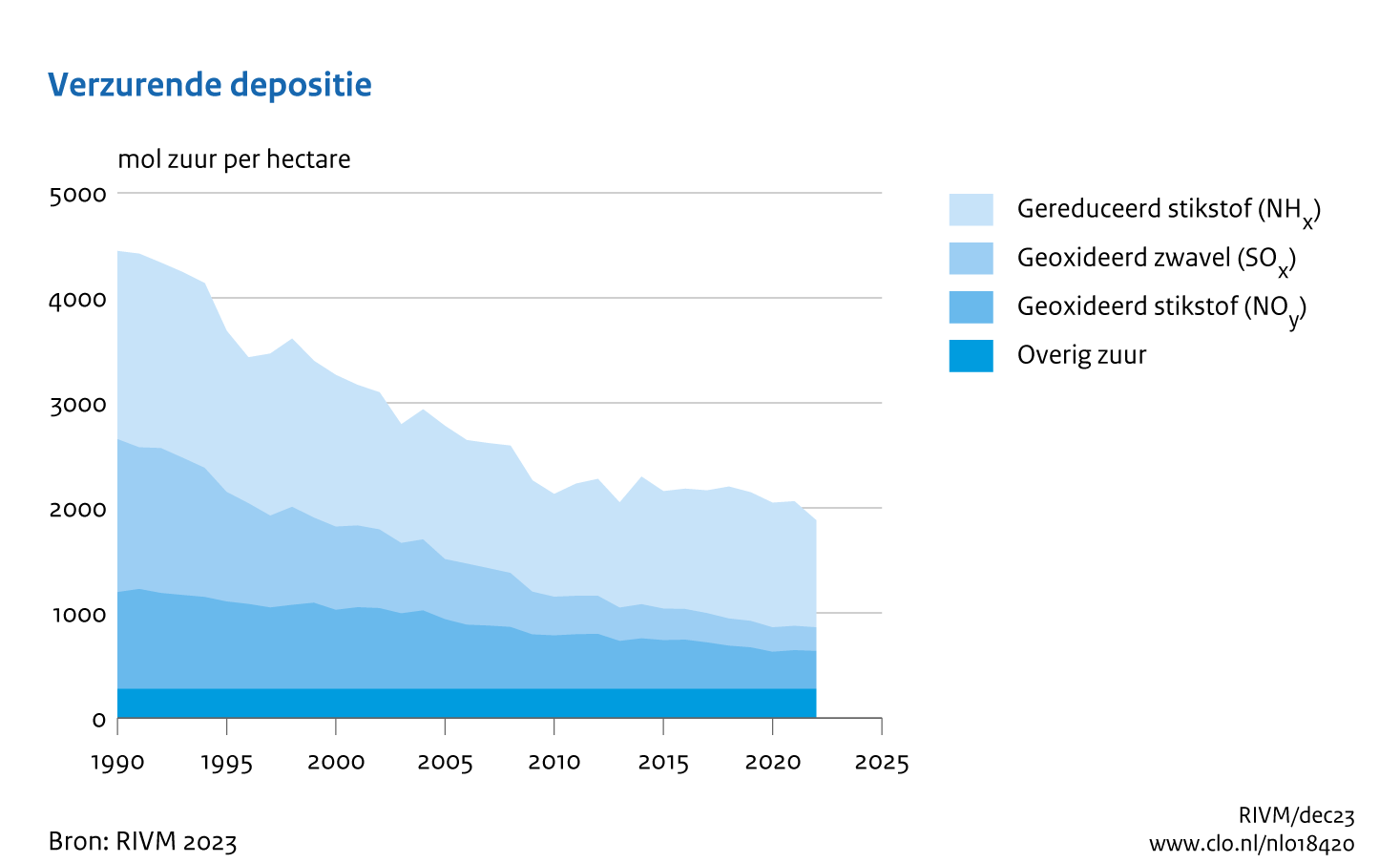
Dit illustreert hoe kleine hoeveelheden metalen in de atmosfeer kunnen leiden tot een fotochemische cyclus die hydroxylradicalen produceert die er op hun beurt weer voor zorgen dat CO, SO2 en NOx in de atmosfeer worden omgezet. De geproduceerde H2SO4 en HNO3 lossen op in water, waarmee zure regen een feit is. Volgens het Compendium voor de Leefomgevingw is de verzurende depositie in Nederland sinds 1990 met 55% afgenomen, zie onderstaande figuur, en is dat vooral te danken aan vermindering van de uitstoot van zwaveldioxide.
Laatste wijziging: 25-04-2024

Deze publicatie valt onder een Creative Commons licentie. Zie hiervoor het colofon.

Deze publicatie valt onder een Creative Commons licentie. Zie hiervoor het colofon.